国家药品监督管理局
备案流程文字说明
第一步:备案资料提交
第二步:备案资料整理
第三步:备案公示
第四步:备案后核查
流程图
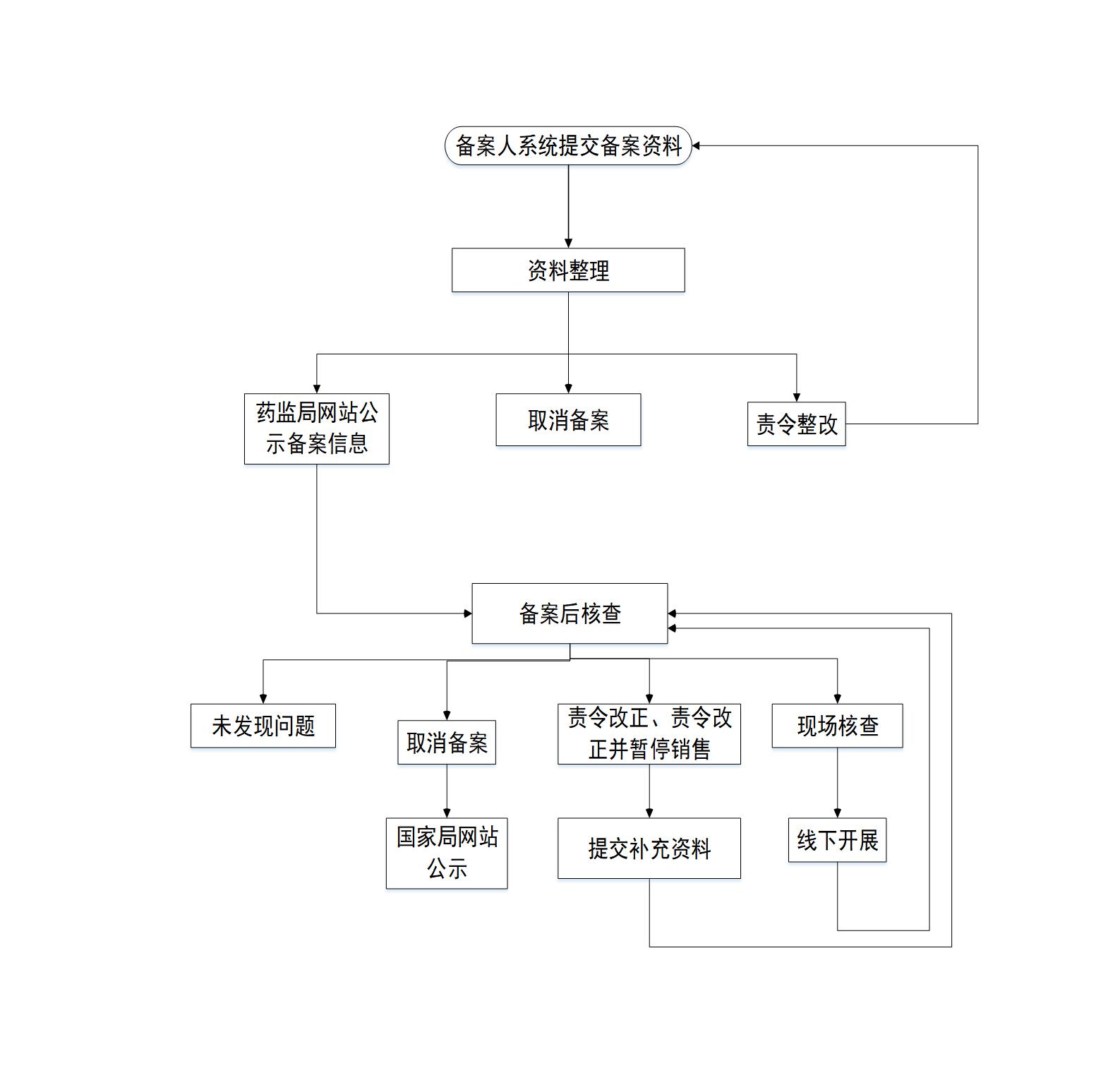
以下是针对中国化妆品新原料备案与注册咨询服务的标准化流程,该流程基于《化妆品监督管理条例》及NMPA最新要求制定,确保专业、高效地完成新原料准入:
化妆品新原料备案/注册咨询全流程
第一阶段:原料预评估与策略制定(耗时:2-4周)
-
原料初步筛查
-
成分安全性预评估(核查CIRS、IUCLID等全球数据库)
-
国内外使用历史调研(食药同源、化妆品使用历史证明)
-
化学结构特性分析(CAS号确认、异构体识别)
-
-
注册路径判定
-
判定标准:
-
备案制:具有安全食用/使用历史的原料
-
注册制:防腐/防晒/着色/染发/祛斑美白/防脱发原料及高风险新原料
-
-
-
制定注册方案
-
确定毒理学测试项目(基于《化妆品新原料注册备案资料管理规定》)
-
编制项目时间表(常规备案6-8个月,注册12-18个月)
-
预算评估(备案制:15-35万元;注册制:40-100万元)
-
第二阶段:技术资料准备(耗时:3-6个月)
-
核心资料编制
-
原料理化性质报告(纯度、稳定性、溶解度等)
-
生产工艺流程图(提供反应方程式、质量控制点)
-
原料质量规格要求(建立企业标准)
-
-
安全性证据收集
-
毒理学测试(必做项目):
-
皮肤刺激性/腐蚀性试验
-
皮肤致敏性试验
-
体外遗传毒性试验(Ames+微核)
-
亚慢性经皮毒性试验(28天)
-
-
可选减免项目(如符合条件):
-
重复剂量毒性试验
-
生殖发育毒性试验
-
毒代动力学试验
-
-
-
测试机构对接
-
推荐NMPA认可实验室(中国疾控中心、上海市皮肤病医院等)
-
监督测试过程(确保符合GLP规范)
-
审核测试报告(数据合规性审查)
-
第三阶段:系统申报与审评跟踪(耗时:2-4个月)
-
平台填报
-
化妆品注册备案信息服务平台账户注册
-
按模块提交资料:
-
基本信息(原料名称、CAS号、分子式)
-
生产工艺简述
-
使用目的和使用范围
-
安全使用量限值
-
-
-
审评跟进
-
备案制:形式审查(5个工作日内公示)
-
注册制:技术审评(90个工作日+补充资料时间)
-
专业应对审评问询(技术问题回复)
-
第四阶段:获批后管理(持续服务)
-
安全监测期管理(3年)
-
编制年度报告模板
-
不良事件记录与报告
-
使用情况统计分析
-
-
信息维护
-
原料报送码申请与管理
-
关联产品注册支持
-
配方变更指导
-
特色服务保障
专业支持体系
-
法规预警服务
-
月度法规更新简报
-
重大政策解读会议
-
合规性影响分析
-
-
技术文档质量管控
-
三级审核制度(技术顾问→法规专家→质量负责人)
-
符合CTD格式要求
-
中英文版本同步准备
-
创新原料专项服务
-
优先审评通道申请
-
符合《支持化妆品原料创新若干规定》的原料
-
中医药特色植物原料
-
生物技术原料(发酵/细胞工程)
-
-
测试方案优化
-
动物试验替代方法应用
-
QSAR分析评估
-
交叉参照(Read-across)策略
-
交付成果清单
-
阶段性交付
-
原料注册可行性报告
-
完整的注册备案资料包
-
审评问询回复意见书
-
-
最终交付
-
新原料备案凭证/注册批件
-
原料安全信息报送码
-
合规使用指南
-
服务优势
-
成功率保障
-
备案制:95%以上成功率
-
注册制:80%以上成功率
-
审评补正指导(不限次数)
-
-
时效保障
-
资料编制超时赔付
-
关键节点短信提醒
-
专家加急服务可选
-
本流程适用于2025年最新监管要求,具体实施将根据原料特性和最新政策动态调整。建议在项目启动前进行详细的原料预评估,以确保选择最优的注册路径和测试方案。





























 18576401396
18576401396